斑马鱼作为模式生物的核心生物学特性与科研应用价值分析
斑马鱼(Danio rerio)是当前生命科学领域极具优势的模式生物,其兼具体型小巧、繁殖高效、发育快速、遗传保守性高及实验操作便捷等核心特质,既能适配高通量实验需求、大幅降低科研成本与周期,又能通过基因编辑技术快速构建疾病模型,有效衔接体外实验与高等哺乳动物体内实验,在药物研发、疾病机制研究、食品化妆品安全性评价及发育生物学等领域展现出不可替代的科研应用价值,已成为推动基础研究向临床转化的关键工具。
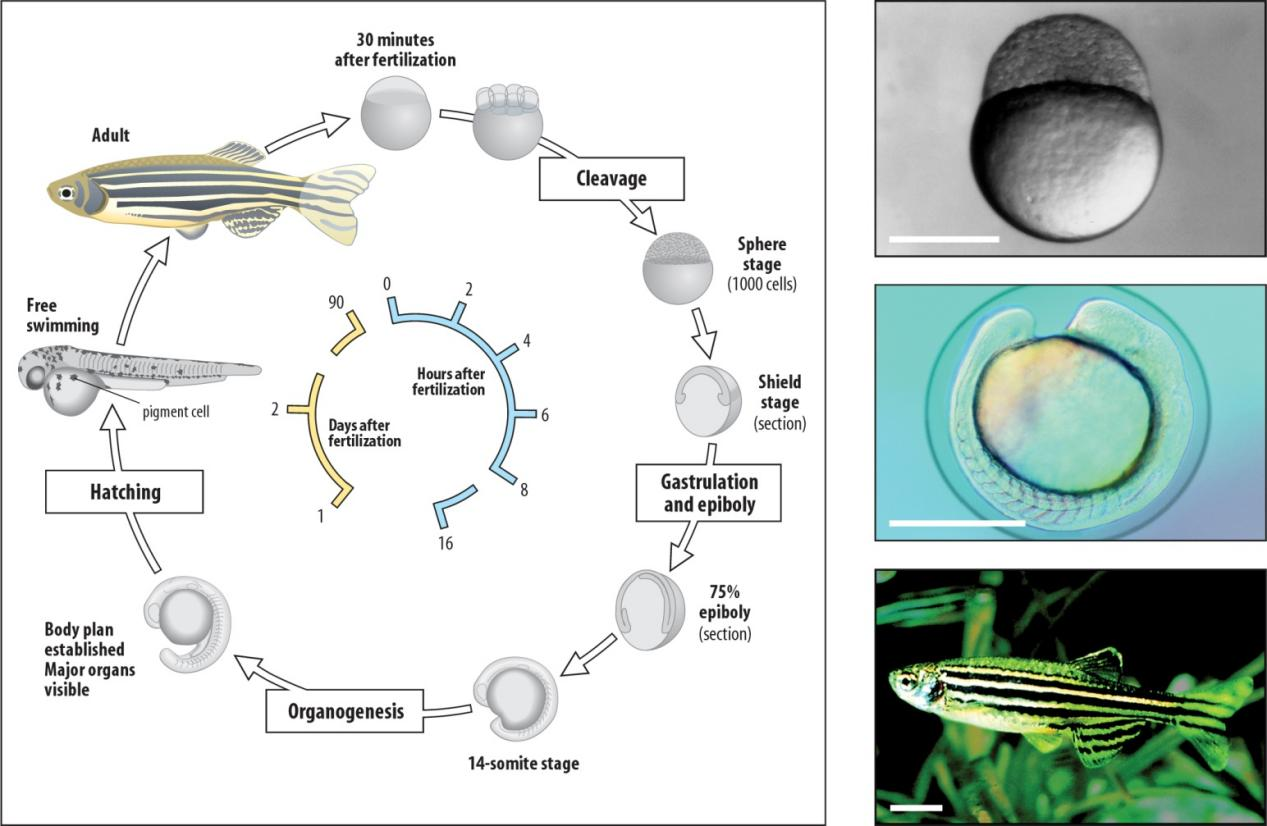
一、核心生物学特性与实验适配优势
(一)体型与实验操作适配性
斑马鱼(Danio rerio)具有显著的体型优势,其幼鱼体长仅为 1–3mm,个体尺寸与 96 孔微孔板的孔容规格高度匹配,可实现基于微孔板的高通量全自动化实验分析,满足大规模样本平行检测需求,显著提升实验效率。
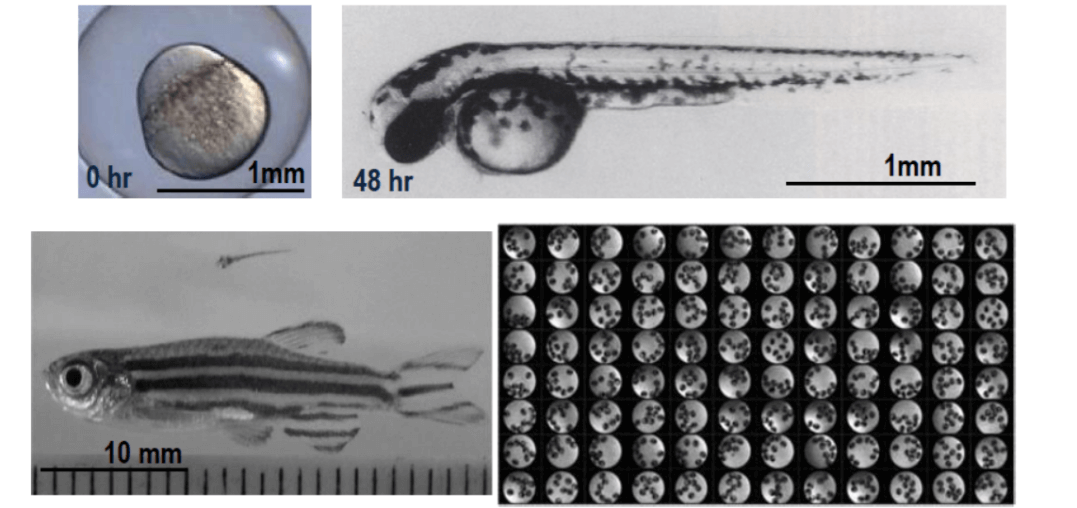
理想的高通量药物筛选模型
(二)养殖成本与空间效益
空间利用率高:在标准化养殖条件下,100㎡养殖空间可承载 30000 只成鱼,单位空间养殖密度远高于传统哺乳类模式生物(如小鼠、大鼠),大幅降低实验室空间占用成本。
综合成本可控:从饲料消耗、水质维护到环境调控的全养殖周期成本,显著低于高等哺乳动物,适合长期规模化实验种群维持。
(三)药物实验资源需求特性
在药物筛选与毒性评估实验中,斑马鱼对药物的需求量极低,仅需微克(μg)级剂量,约为啮齿类动物(如小鼠)实验用药量的 1/100–1/1000,可大幅减少药物样品消耗,尤其适配早期药物研发阶段的微量样品检测场景。
(四)样本获取与繁殖特性
体外发育特性:斑马鱼胚胎及幼体均在体外完成发育,无需侵入性操作即可直接观察发育过程,且样本获取便捷,可快速获得大量用于生物医学研究及药物实验的标准化动物样本。
高繁殖力:雌性斑马鱼具有稳定的高产卵能力,单只雌鱼每周产卵量可达 300–500 枚,全年无明显繁殖休眠期,可保障实验样本的持续、稳定供应,满足长期实验需求。
(五)发育进程与观察优势
快速发育周期:斑马鱼胚胎发育速度快,受精后 24 小时(24 hpf)即可完成主要器官原基的构建;受精后 2–5 天(2–5 dpf),心脏、脑、血液系统、血管网络、胰腺、肝脏等与人类同源的关键器官已具备功能活性,可快速进入实验观察窗口期。 透明化观察便利:受精后前 7 天(7 dpf)的斑马鱼幼体通体透明,内部器官结构清晰可见,且可直接观察到节律性心跳(约 120–180 次 / 分钟)与血液循环过程,无需复杂染色或解剖操作即可实现动态生理过程监测,降低实验干扰。
(六)实验周期优势
基于快速发育特性,斑马鱼相关实验的周期显著缩短,多数药物筛选、毒性评估及发育表型分析实验可在 1–2 周内完成;而传统哺乳类动物体内实验(如小鼠药效实验)通常需 1 个月以上,大幅提升科研项目推进效率。
(七)遗传保守性与人类疾病关联性
斑马鱼与人类的疾病信号转导通路具有高度进化保守性,其基因组中与人类的同源基因比例高达 87%,其中部分疾病相关关键基因(如肿瘤、心血管疾病相关基因)的保守性可达 99%。这一特性确保了斑马鱼模型中药物作用机制研究、疾病病理模拟的结果,可有效外推至人类生理病理系统,提升实验结果的转化价值。
二、科研应用定位与技术赋能
(一)模型生物的核心应用领域
斑马鱼模型有效弥补了传统体外实验(如细胞系实验)与人类体内生理环境可比性差的缺陷,同时规避了高等哺乳动物(如灵长类、啮齿类)体内实验周期长、成本高、伦理审查严格的局限,已成为人类疾病机制研究、活体高通量药物筛选的核心模式生物之一,同时在发育生物学、组织器官再生、神经生物学、心血管疾病模型构建等领域广泛应用。
(二)基因编辑技术的协同赋能
依托 CRISPR/Cas9基因编辑技术的成熟应用,可在斑马鱼体内实现高效、精准的基因敲除、敲入及点突变,最快可在5-6个月内完成个性化基因定制模型构建,为基因体内功能验证、疾病(如遗传性疾病、肿瘤)模型建立及药物作用机制解析提供高效技术支撑,进一步拓展了其在精准医学研究中的应用边界。


